pGX9501是中国首个进入临床阶段的DNA新冠候选疫苗。其是以SARS-CoV-2为靶标的DNA候选疫苗,可编码合成与野生型SARS-CoV-2序列相匹配(氨基酸序列一致性超过99.9%)的全长刺突蛋白序列(刺突蛋白是SARS-CoV-2的主要表面抗原)。接种疫苗后,pGX9501质粒可以转录成mRNA并进一步翻译成可编码的蛋白质,从而激活免疫系统以产生免疫应答。pGX9501具有潜在的良好免疫原性、更好的安全性和耐受性,其先进的生产工艺和强大的稳定性,为该项目提供了与其他已批准和正在开发的COVID-19疫苗差异化特质。艾棣维欣自2020年1月以来,与战略合作伙伴美国Inovio制药共同开发pGX9501,共同进行了临床前研究、早期临床试验等。目前,公司已经在国内完成了pGX9501的I期和II期临床试验,以及加强针的探索性临床试验。
2021年10月,pGX9501/INO-4800入选由世卫组织独立开展的一项大型国际随机对照III期临床试验,该试验被称为团结试验疫苗(STV),目前仅有两种疫苗入选。此次试验由世卫组织和每个参与国家的卫生部共同发起。STV计划旨在快速评估新的候选疫苗的有效性和安全性,为保护全球人类免受COVID-19感染所需的更大疫苗需求作出贡献。

ADV1101是公司针对新冠病毒变异株自主开发的预防性疫苗。公司基于对新冠病毒各变异株的研究,开发了广谱的疫苗ADV1101。目前该产品处于临床前阶段。
与pGX9501相比,ADV1101能够更好地对新冠各个变异株的感染提供保护,展现了产品广谱优势。此外,ADV1101疫苗的递送是基于公司与青澜生物共同开发的微针递送技术,微针技术相较于现有的DNA疫苗递送技术,具备更好的使用便利性和依从性。
ADV2301是公司针对新冠病毒开发的单克隆抗体,目前该产品处于临床前阶段。
由于新冠病毒有较高的变异频率,大量变异毒株的变异多出现在S蛋白上,即中和抗体的结合表位,导致针对之前新冠病毒开发的中和抗体失去中和活性。因此,筛选找到不易受病毒变异的影响的中和保守抗原表位的抗体非常重要。公司在动物试验中检验了ADV2301抗体的效果,动物试验结果显示ADV2301具备对新冠病毒及各变异株的中和能力,尤其对Omicron BA.2及BA.4/5等毒株具备较强的中和效力。
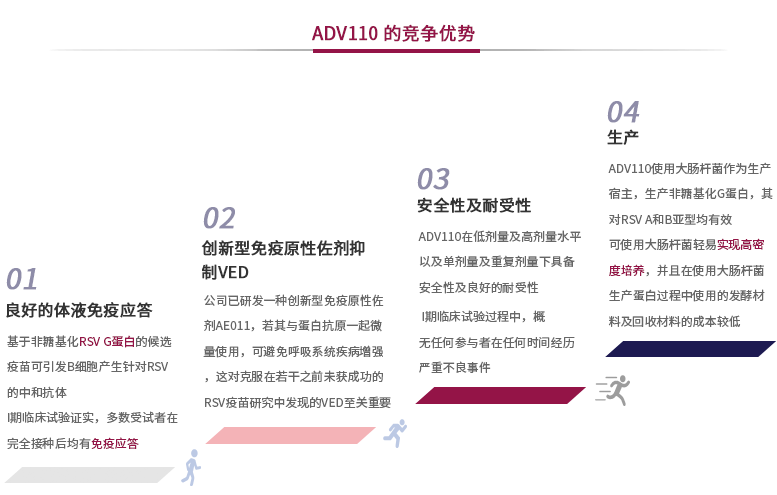
一种含有新型佐剂的潜在首创RSV蛋白亚单位候选疫苗,旨在保护6个月至5岁的儿童及65岁以上的老年人。ADV110由两种活性成份按照优化比例组成。两种活性成分分别是:(1)纯化的RSV G蛋白亚单位(作为免疫原性成份)及;(2)公司自主开发的佐剂AE011(使用微量环孢霉素A时可作为免疫调节剂及RSV G蛋白的稀释剂)。迄今为止,我们的ADV110是唯一由中国公司设计开发的处于临床阶段的RSV候选疫苗,也是全球临床最先进的疫苗之一。我们亦是在临床阶段在RSV疫苗中使用新型佐剂作为免疫调节剂的先驱,此举有可能扩展佐剂传统功效(增强疫苗免疫应答)之外的用途。我们已开始就在澳大利亚进行的II期临床试验进行受试者招募准备工作。
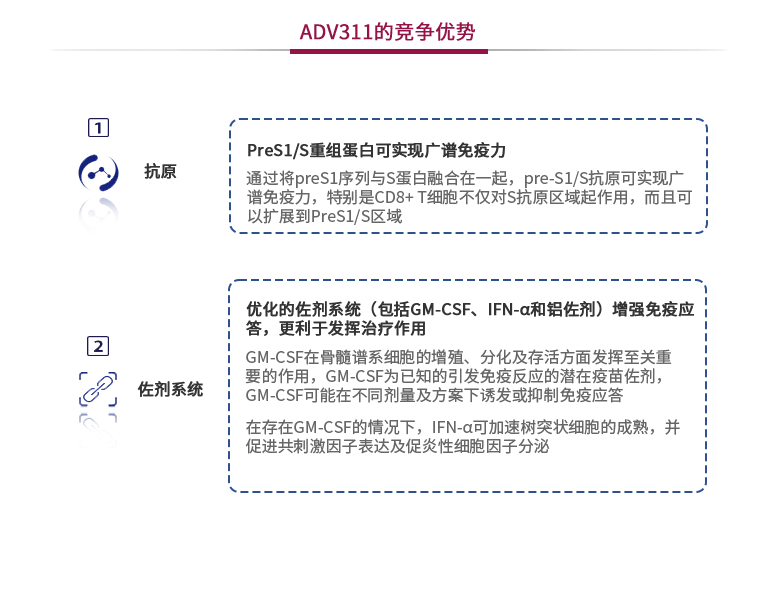
乙型肝炎是由乙肝病毒引起的广泛的传染性肝病,可引起并发症,例如肝硬化、肝衰竭及肝癌。众所周知,乙肝患者存在较高的疾病负担,包括社会污名、劳务损失及沉重的经济负担。ADV311为治疗性疫苗,已进入临床前阶段,以实现功能性治愈为目的。ADV311由源自Large HBsAg(为一种乙肝表面抗原)的PreS1/S重组蛋白及CA02的佐剂系统组成。佐剂系统具体包括GM-CSF(粒细胞-巨噬细胞集落刺激因子)、IFN-α(一种细胞因子)及铝佐剂。
ADV520是公司针对肿瘤开发的基于肿瘤相关抗原(TAA)的治疗性候选疫苗,目前该产品处于临床前阶段。TAA是肿瘤特异性抗原,可通过人类白细胞抗原(HLA)呈递并被宿主免疫系统识别,从而激活特异性T细胞并诱导抗肿瘤免疫应答以抑制肿瘤生长。ADV520利用与肿瘤相关的编码为GN011的抗原基因,结合公司专有的新型佐剂系统,可以进一步的增强宿主抗肿瘤免疫力。一般认为,GN011是一种胎儿蛋白,在胎儿期高度表达,出生后迅速关闭,但在肿瘤期重新活化。因此,GN011靶标可能是癌症疫苗的新候选疫苗。
ADV610是公司针对突变肿瘤开发的基于突变抗原的治疗性候选疫苗。由于癌症突变抗原在癌症中的表达率高,在正常的体细胞组织中缺乏表达,从而具有很高的免疫原性。突变抗原对每个患者都具有高度特异性,因此,对突变的抗原进行快速测序及分析是开发有效的基于突变抗原的抗肿瘤治疗性疫苗的关键。公司正在利用DNA疫苗技术平台及已建立的内部方案开发ADV610,以进行快速序列设计及优化。公司还计划使用佐剂进一步提高ADV610的疗效。目前该产品处于临床前阶段。